高中化学的问题
已知Ca3(PO4)2、CaHPO4均不溶于水,且Ca3(PO4)2的溶解度比CaHPO4的溶解度小。将0.05 mol·L-1 Ca(H2PO4)2溶液与0.15 mol·L-1 NaOH溶液等体积混合,搅拌后静置,充分进行反应。请写出反应的离子方程式:为什么这个离子方程式这么写?
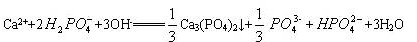
主要是考察反应物过量的问题,当NaOH过量时,会发生2个反应Ca(H2PO4)2~2NaOH;CaHPO4~NaOH。可认为前者先反应,反应完全后再发生后面的反应。由于加的Ca(H2PO4)2:NaOH的物质的量之比=1:3,显然2个反应都发生,且参与前后的NaOH之比为2:1。假设跟后者反应的NaOH物质的量为x,前者就是2x,在根据反应方程式分别解出产物,求比值,就得到了上面的离子方程式
热门标签: